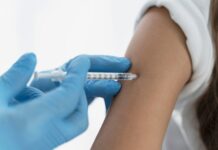
Дни след като прикова вниманието към себе си със своята „ваксина срещу COVID-19 за света“, компанията „AstraZeneca“ е изправена пред сложни въпроси относно степента на успеваемост, които според някои експерти могат да попречат на шансовете ѝ за бързо одобрение от регулаторните органи на САЩ и ЕС. Няколко учени изразиха съмнения относно надеждността на резултатите, показващи, че ваксината е 90% ефективна при една от подгрупите от участници в клиничните проучвания, които първоначално по грешка са получили половин доза, последвана от пълна доза.
„Това, което трябва да продължим да правим, е да събираме данни.“, заяви Питър Опеншоу, професор по експериментална медицина в „Imperial College“ в Лондон.
„Трябва да изчакаме да излязат пълните данни и да видим как регулаторите гледат на резултатите.“, каза той и добави, че е твърде вероятно американските и европейските регулаторни органи да заявят различни позиции по въпроса.
Британският производител на лекарства „AstraZeneca“ заяви, че неговата експериментална ваксина, разработена съвместно с Оксфордския университет, предотвратява средно 70% от случаите на COVID-19, което е потвърдено от късните етапи на клиничните проучвания във Великобритания и Бразилия. Докато процентът на успеваемост е бил 90% при подгрупата на доброволците, ефикасността е била 62%, ако пълната доза е приложена чрез две дози два, както при повечето участници. Това е доста над 50% ефикасност, изисквана от американските регулатори.
Европейският регулаторен орган по лекарствата заяви, че засега няма да постанови какъв да бъде процентът на минимално ниво на ефикасност за потенциалните ваксини. В основата на притесненията обаче е фактът, че най-обещаващият резултат от проучването от 90% е получен от анализ на подгрупа – техника, която според много учени може да даде невярна информация.
„Анализите на подгрупи в рандомизирани контролирани проучвания винаги са изпълнени с трудности.“, твърди Пол Хънтър, професор по медицина в Британския университет в Източна Англия.
Той обясни, че подобни анализи увеличават риска от „грешки тип 1“ – с други думи, когато дадена интервенция се счита за ефективна, а всъщност не е такава. Това е отчасти защото броят на участниците е значително намален в една подгрупа, което пък на свой ред прокрадва идеята дали констатацията не се свежда само до случайни разлики или прилики в показателите на участниците.
Дяволът се крие в детайлите
„AstraZeneca“ заяви, че прилагането на половината доза е прегледано и одобрено от независими лица, които следят процесите по безопасност и регулаторния орган на Обединеното кралство, като добави, че регулаторът публично е потвърдил, че „няма поводи за притеснение“.
Засега Оксфордският университет не е дал коментар по въпроса. Американският регулатор, Администрацията по храните и лекарствата (FDA) също все още не заявила позицията си относно резултатите от клиничните тестове на ваксината на „AstraZeneca“. Европейската агенция по лекарствата заяви вчера, че ще оцени данните за ефикасността и безопасността на ваксината през следващите седмици, след като те бъдат предоставени от компанията. Въпреки това в регулаторния процес има спънки, смятат някои експерти, които отбелязват критични пропуски в данните, които „AstraZeneca“ е публикувала досега. „Дяволът е в детайлите“, каза Дани Алтман, професор по имунология в „Imperial Collegе„.
„Опитваме се да направим оценка на наистина доста сложни дизайни на проби въз основа на кратки съобщения за пресата.“ Освен изявленията на степента на ефикасност публикувани от „AstraZeneca“, не са предоставени други ключови данни, които учените да анализират. Не се казва колко инфекции са възникнали в подгрупата, особено при доброволците, които са получили две пълни дози, или в групата, при която е бил приложен плацебо ефектът.
Много променливи величини
Монсеф Слауи, главен научен съветник на програмата за ваксини на правителството на САЩ „Operation Warp Speed“, също подчерта пропуските. Той каза, че никой в подгрупата, получил първоначалната половин доза, не е по-възрастен от 55 години, с което се предполага, че ефективността на продукта при по-възрастни групи не е доказана в тези междинни данни.
В групата, която е получила правилната пълна доза, последвана от още една пълна доза, са участвали и възрастни хора. „Има редица променливи, които трябва да разберем правилно, както и каква е ролята на всяка от тях за постигане на разликата в ефикасността.“, каза Слауи по време на брифинг във вторник. „Все пак е възможно разликата в ефикасността да е случайна.“, добави той. „Това е малко вероятно, но все пак е възможно.“